電台訪問
聖諾醫藥(2257)是香港政府引進來的重點企業,公司憑藉在RNA療法及新型遞送平台技術方面的豐富經驗,建立起豐富的臨床管線。聖諾醫藥董事會主席、執行董事、總裁兼首席執行官陸陽博士在接受新城財經台《企業藍圖》上市公司專訪的時候表示,聖諾醫藥在治療腫瘤方面,用作治療非黑色素瘤皮膚癌的候選藥物STP705以及STP707已經完成了美國食品藥品監督管理局(FDA)的二期臨床研究,目前正在推進臨床三期的工作。按照既有方法穩步前進,預計大概在兩年半到三年的時間,藥物可以進入到市場。當然,公司亦會繼續和大型醫藥企業合作,吸引資金投入,在管線和技術的上面實現利潤。另外,聖諾醫藥亦開拓了醫學美容方面的應用,執行董事、首席戰略官戴曉暢博士指出STP705的藥物可以嘗試用在醫學減脂塑型方面,目前正開展一期臨床試驗,成功推出的話,將會進行全球銷售。(撰文:朱明亮)
聖諾醫藥Sirnaomics在2007年成立,是一家小核酸藥物又稱作RNAi(核酸干擾,RNA interference)技術藥物公司。RNA療法,是一種使用基於核糖核酸分子來治療或預防疾病的新療法,包括用於治療和疫苗開發的RNAi、mRNA以及RNAe(RNA編輯)技術。近年來,隨著mRNA新冠疫苗的成功研發以及廣泛使用,使得RNA技術亦逐步為大眾認識。而mRNA只是RNA藥物矩陣當中的一眾,隨著靶點發現技術的進步、遞送技術的成熟,RNA藥物仍有很大的發展空間與潛力。

被稱為「亞洲RNA療法第一股」,陸陽表示,聖諾醫藥在中美都有深度布局,美國總部在華盛頓郊區,而中國內地就在蘇州、廣州及香港等地設立辦公室以及研發基地。目前聖諾醫藥以及非全資附屬公司RANimmune和EDIRNA在香港設立了辦公室,並且已經進駐了香港科技園,目標是在香港進行RNA療法相關的研發和臨床研究合作,另外探討在落馬洲河套地區建立具商業規模的生產計劃。
陸陽介紹道,聖諾醫藥在中美兩地都有扎實的研發團隊,總體人數過百名,研發團隊有非常資深藥物開發領域、不同階段的專家。而且美國的團隊更具有國際一流水平,特別是在核酸製藥領域。而蘇州方面則有早期團隊,有新藥、成藥創製整個工藝規範化生產的團隊。他相信,中美兩地的團隊可以有很好的互補性,並且具有國際視野。
公司產品管線涵蓋腫瘤學及纖維化相關疾病以及抗病毒及心臟代謝疾病,以及流感、乙型肝炎、HPV及新冠病毒感染;心血管代謝疾病的治療;胰腺癌、結腸癌、其他癌症;及醫美脂肪塑性等。
廣州灌裝廠滿足內部測試需求
面對越來越多管線產品的臨床試驗對試劑需求增加,聖諾醫藥在2021年就建造了廣州的灌裝工廠,並且成功運營一年。
廣州的灌裝廠主要服務於聖諾醫藥內部測試,而且聖諾掌握了相關的技術專利。現在工廠的產能已經可以達到當初設定的目標,已經有三個產品11個批次的灌裝產品推出,目前正進行第四個品種的生產。
陸陽透露,按照設計標準,廣州灌裝廠可以生產16萬支固體製劑以及60萬支液體製劑,目前產能尚未達到最高的設計劑量產出,但如果有進一步需求,可以通過人員調整及進程優化,達到設計的水平。
擬香港推進RNA療法及臨床研究
根據目前的產品管線進度,聖諾醫藥在腫瘤學方面的候選藥物STP705的進度最快,已經完成了FDA的二期臨床試驗,並且積極推進三期臨床試驗。
聖諾醫藥的STP705主要用於非黑色素瘤皮膚癌的治療。據資料介紹,基底細胞癌(BCC)及鱗狀細胞癌(SCC)佔非黑色素皮膚癌的大部分,估計美國每年產生的新診斷病例超過500萬例。非黑色素瘤皮膚癌是常見的三種皮膚癌之一,又稱為鱗狀細胞癌,鱗狀細胞癌比較容易發生轉移。如果太遲發現會入侵血管和淋巴管,再轉移到其他的器官,即使於此時進行手術切除也有復發的可能。
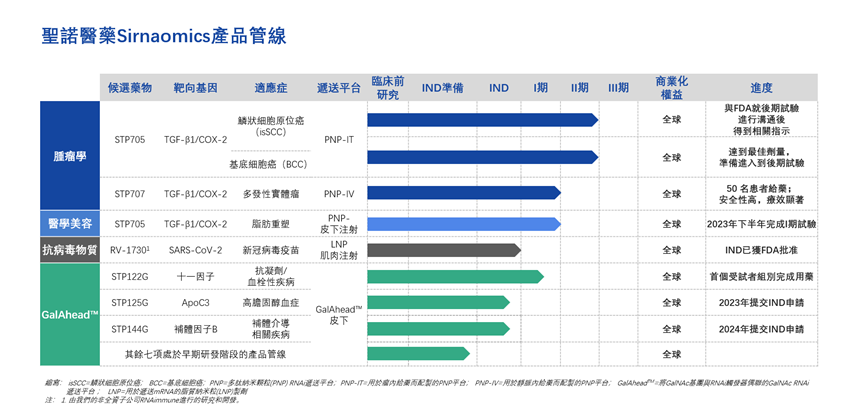
戴曉暢指出,STP705是一種雙靶點抑制劑藥物,用於局部給藥,在治療非黑色素瘤皮膚癌有積極的臨床數據。之所以是雙靶點,是因為腫瘤往往會逃逸,兩個靶點的時候會增加逃逸的難度,目前非黑色素瘤皮膚癌雖然香港少見,但在全球一個非常廣泛的疾病,例如美國、歐洲、澳洲及中東地區病例非常多。
陸陽指,公司正在和美國FDA緊鑼密鼓溝通STP705的進度,並且希望在溝通後獲得第三期的相關指示。他預計在一般情況下,穩步推進三期研發,可以在兩年半到三年時間,將藥物推向市場。當然,若完成小三期臨床試驗後結果理想的情況下,可以向FDA申請加快審評,這個過程需要一年半到兩年時間。
陸陽補充,三期臨床試驗將會以美國為主,是一個全球多中心的一個三期臨床試驗,此外還考慮包括東南亞、香港、新加坡和中東進行測試,當然還包括澳大利亞和南歐。
除了STP705可以進入三期臨床測試,聖諾醫藥目前的STP707進度亦較快,戴曉暢博士解釋,STP707是用於全身給藥的,用作實體腫瘤,例如肝癌、腎癌、膽管癌這一類特別難治療的實體腫瘤。
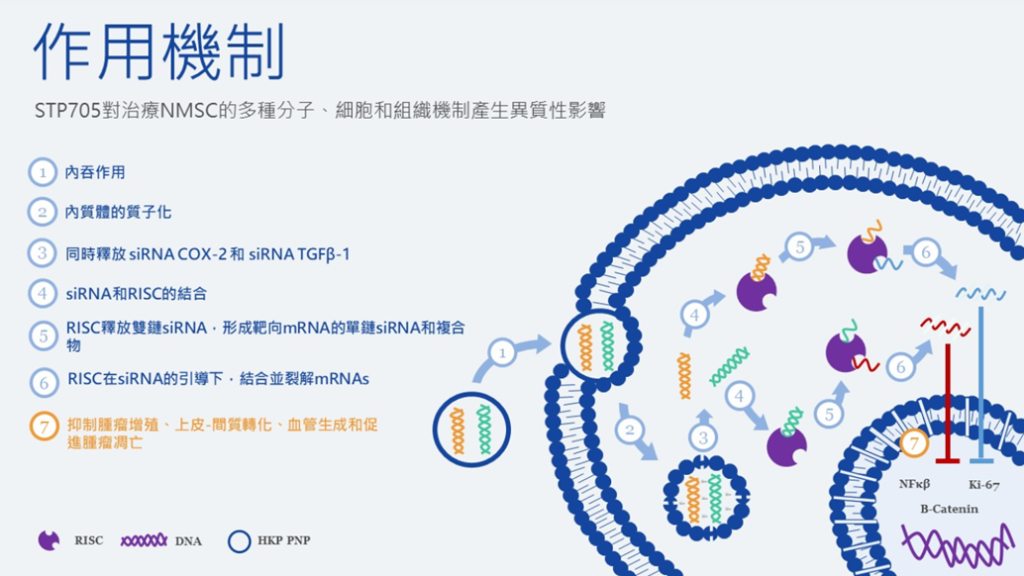
由於STP705的研發較為順利,並且在此技術的基礎上發現了STP705可以用於腹部整形術患者脂肪重塑,並且相關的一期臨床試驗數據在今年6月已經公開。聖諾醫藥計劃將候選藥物用於局部脂肪重塑,並且用於頦下脂肪的治療以非侵入性脂肪重塑的其他領域。
戴曉暢解釋道,STP705 局部塑形主要用在雙下巴局部減脂,原理是讓脂肪細胞縮小,改變脂肪的代謝,現在關於醫美的產品正在做一期臨床試驗,而且同樣需要三期的臨床通過了才可以推出,未來會進行全球推廣。
預計2025年可以實現產品銷售
作為生物醫藥企業,目前聖諾醫藥已經進入後期臨床階段。聖諾醫藥在2021年底上市,集資淨額約4億元。公司2022年全年錄得虧損8,830萬元,今年上半年錄得虧損4,110萬元,比去年同期虧損4,610萬元有所減少,絕大部分的虧損來自研發開支及行政開支。
陸陽表示,聖諾醫藥實現利潤成效,不僅僅是在產品出售方面,而且是在企業下一步和大型醫藥企業合作,本身就會吸引很多資金的投入。甚至可以說,是一個技術和產品管線的銷售。
陸陽指出,在GalAheadTM遞送技術平台技術基礎上,目前有STP122G、STP125G、STP144G等候選藥物,分別用於治療抗凝血和血栓性疾病、高膽固醇血症、補體介質相關疾病。其中STP122G已經獲得美國FDA的監管許可,並且開始進入一期臨床試驗。
今年上半年,聖諾醫藥已經成功將GalAheadTM遞送平台首個代表性候選藥物STP122G推進至臨床階段,並且提交了新型mRNA疫苗的新藥臨床試驗研究申請(IND),此外,公司正加快下一代GalAheadTM平台的研發。
對於接下來的公司部署,陸陽透露聖諾醫藥還在推進與高血壓相關的長效抑制劑的技術領域,而且會考慮推進新的技術例如考慮中樞神經疾病的治療等。
想了解更多關於聖諾醫藥的發展情況,歡迎收聽本期企業藍圖。
【關於 #企業藍圖】
《企業藍圖》為新城財經台《104投資總部》環節,節目逢星期日晚上11:30-12:00播出。《企業藍圖》主要訪問上市公司管理層,透過訪問深入不同行業的發展趨勢,了解公司的財務狀況、盈利模式、營銷策略以及未來發展部署。除了上市公司外,節目亦會訪問初創企業以及在各領域有傑出表現的公司。








 更新時間: 2025-07-02
更新時間: 2025-07-02  更新時間: 2025-07-02
更新時間: 2025-07-02 




